Introduzione: la marcatura laser come processo critico
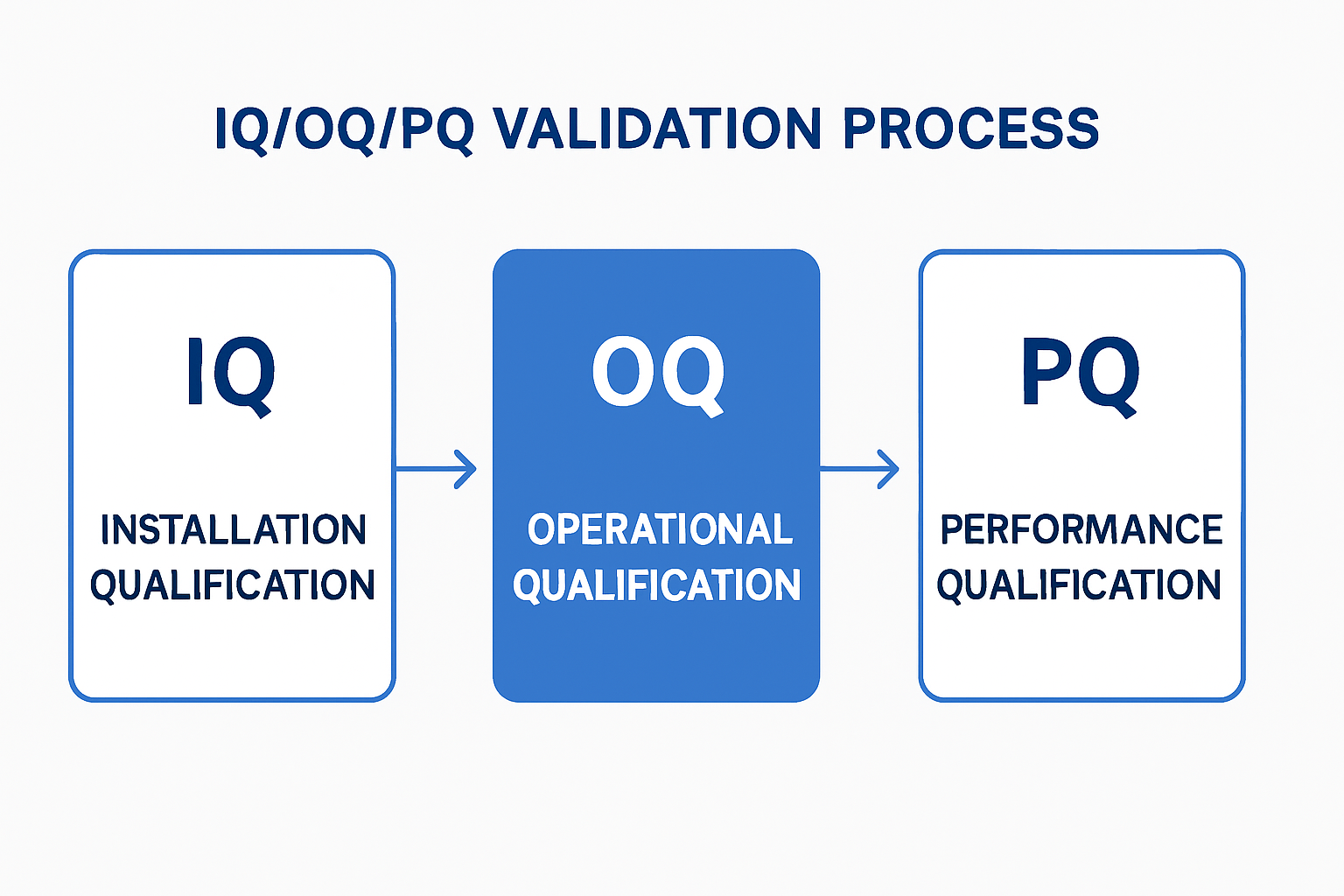
Per i produttori di dispositivi medici, la conformità al regolamento statunitense sull’Identificazione Unica del Dispositivo (UDI) della Food and Drug Administration (FDA) è obbligatoria. Il sistema UDI richiede una marcatura permanente e leggibile sul dispositivo o sul suo imballaggio, al fine di migliorare tracciabilità dei dispositivi medici e la sicurezza del paziente. Poiché la marcatura laser è un processo produttivo che influisce direttamente sulla qualità del prodotto finale e sulla conformità normativa, l’attrezzatura e il processo stesso devono essere rigorosamente convalidati secondo i regolamenti del sistema qualità (QSR) e ISO 13485 le norme applicabili. Questo articolo illustra dettagliatamente il processo di convalida essenziale in tre fasi: Qualifica dell’Installazione (IQ), Qualifica Operativa (OQ) e Qualifica delle Prestazioni (PQ).
1. Qualifica dell’Installazione (IQ): Garantire una configurazione corretta
La fase IQ verifica che l’attrezzatura per la marcatura laser sia stata installata correttamente e che tutti i componenti necessari, le utilities e la documentazione siano presenti.
Principali attività IQ:
-
Verifica dell’attrezzatura: Conferma che l’attrezzatura ricevuta corrisponda alle specifiche indicate nell’ordine d’acquisto (ad es. tipo di laser, potenza, lunghezza d’onda).
-
Revisione della documentazione: Verifica che tutta la documentazione fornita dal produttore, inclusi manuali, certificati di taratura e procedure di manutenzione, sia presente e completa.
-
Controlli delle utilities: Conferma che il sito di installazione fornisce le utilities richieste (alimentazione elettrica, aria compressa, ventilazione di scarico) e che le condizioni ambientali (temperatura, umidità) rispettano le specifiche del produttore.
-
Installazione del software: Verifica che il software per la marcatura e i sistemi di controllo siano stati installati correttamente e che tutti i controlli di sicurezza e di accesso siano configurati in modo adeguato.
Obiettivo della Qualifica di Installazione (IQ): Stabilire che l’attrezzatura è stata installata correttamente nell’ambiente previsto ed è pronta per l’esercizio.
2. Qualifica Operativa (OQ): Definizione della finestra operativa
La fase di OQ stabilisce che l’attrezzatura per la marcatura laser opera in modo coerente all’interno dei campi operativi specificati. Questo passaggio è fondamentale per definire la "finestra operativa sicura" per il processo di marcatura.
Principali attività di OQ:
-
Test dei parametri: Test sistematico dell’intero intervallo di parametri operativi critici, quali potenza del laser, velocità di marcatura, frequenza e distanza di messa a fuoco.
-
Test dello scenario peggiore: Test dell'apparecchiatura ai limiti estremi del campo di funzionamento (ad esempio, potenza minima e massima, velocità massima e minima) per garantire che il sistema continui a funzionare correttamente.
-
Test di allarmi e interblocchi: Verifica del corretto funzionamento di tutte le caratteristiche di sicurezza, degli allarmi e degli interblocchi (ad esempio, interblocchi delle porte, pulsanti di arresto di emergenza, allarmi di guasto del sistema di estrazione dei fumi), conformemente alla progettazione.
-
Test della qualità del marchio: Generazione di marchi di prova su tutto il campo di funzionamento e misurazione degli attributi chiave della qualità (ad esempio, contrasto, profondità, leggibilità del codice) per definire i limiti accettabili.
Obiettivo della qualifica operativa (OQ): Stabilire i limiti operativi e dimostrare che l'apparecchiatura produce risultati accettabili quando viene utilizzata entro tali limiti.
3. Qualifica delle prestazioni (PQ): Dimostrazione di risultati costanti
La fase PQ è l'ultimo e più critico passaggio, che dimostra come il processo di marcatura laser produca in modo costante risultati accettabili in condizioni di produzione reali o simulate per un periodo prolungato. Requisiti FDA per l'UDI relativi alla permanenza e alla qualità della marcatura.
Principali attività PQ:
-
Esecuzione della produzione: Esecuzione di più cicli produttivi utilizzando materiali effettivi e i parametri operativi definiti (stabiliti nella fase OQ).
-
Prove di permanenza della marcatura: Sottoposizione dei dispositivi marcati a condizioni di utilizzo finale simulate, incluse:
-
Cicli di sterilizzazione: Autoclave, ossido di etilene (EtO) o irraggiamento gamma.
-
Pulizia/disinfezione: Esposizione ripetuta a detergenti e ad abrasione.
-
Usura/abrasione: Verifica della resistenza del marchio ai danni fisici.
-
Verifica della tracciabilità: Garantire che i dati UDI impressi sul dispositivo siano correttamente collegati ai registri del lotto di produzione e al database GUDID.
-
Criteri di accettazione: I marchi devono soddisfare in modo costante i criteri di accettazione predefiniti (ad es. livelli AQL per leggibilità, contrasto minimo, assenza di danni al materiale).
Obiettivo della PQ: Dimostrare, con un elevato grado di affidabilità, che il processo di marcatura laser è efficace e riproducibile nelle normali condizioni operative, rispettando tutti gli standard qualitativi e normativi.
Conclusione: un partenariato per la conformità
La convalida di un sistema di marcatura laser è un processo complesso e articolato in più fasi che richiede una profonda conoscenza tecnica e un rigoroso rispetto di ISO 13485 e Requisiti FDA per l'UDI . La scelta di un fornitore di attrezzature laser in grado di offrire un supporto completo per la convalida — inclusi protocolli dettagliati, assistenza nell’esecuzione e relazioni finali — è essenziale per garantire tracciabilità dei dispositivi medici e il conseguimento della conformità normativa. Questo rigoroso processo di convalida IQ/OQ/PQ trasforma il marcatore laser da semplice apparecchiatura in un processo produttivo critico e pienamente convalidato.
Figura 4: Il processo di convalida IQ/OQ/PQ in tre fasi