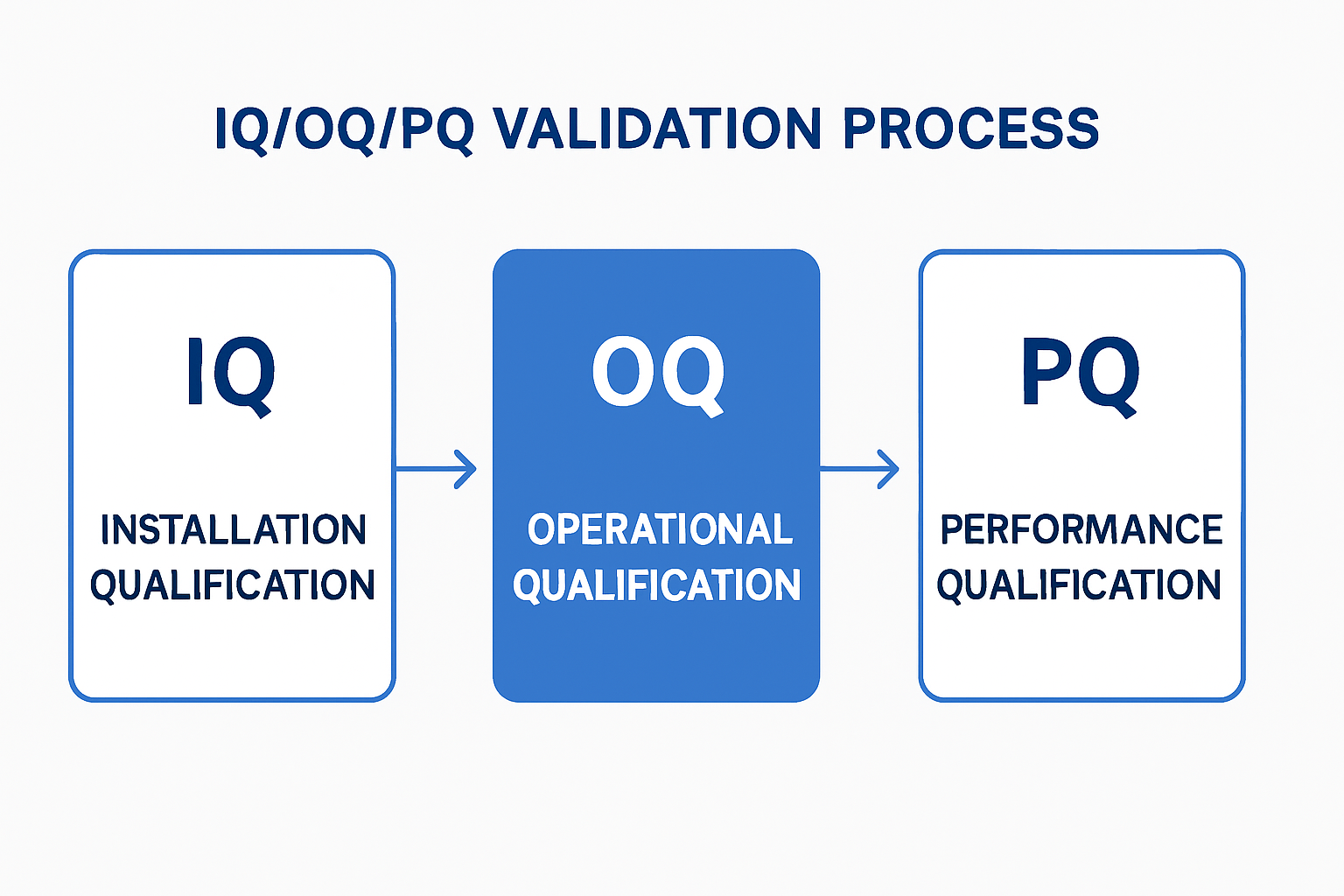
Introdução: A marcação a laser como um processo crítico
Para fabricantes de dispositivos médicos, a conformidade com a regulamentação norte-americana da Food and Drug Administration (FDA) sobre Identificação Única de Dispositivos (UDI) é obrigatória. O sistema UDI exige uma marca permanente e legível no dispositivo ou em sua embalagem para melhorar rastreabilidade de dispositivos médicos e a segurança do paciente. Uma vez que a marcação a laser é um processo de fabricação que afeta diretamente a qualidade do produto final e a conformidade regulatória, o equipamento e o próprio processo devem ser rigorosamente validados de acordo com as regulamentações do sistema de qualidade (QSR) e ISO 13485 normas. Este artigo detalha o essencial processo de validação em três etapas: Qualificação de Instalação (IQ), Qualificação Operacional (OQ) e Qualificação de Desempenho (PQ).
1. Qualificação de Instalação (IQ): Garantindo a Configuração Correta
A fase IQ verifica se o equipamento de marcação a laser foi instalado corretamente e se todos os componentes necessários, utilities e documentação estão presentes.
Principais Atividades da IQ:
-
Verificação do Equipamento: Confirmando que o equipamento recebido corresponde às especificações da ordem de compra (por exemplo, tipo de laser, potência, comprimento de onda).
-
Revisão da Documentação: Verificando se toda a documentação do fabricante — incluindo manuais, certificados de calibração e procedimentos de manutenção — está presente e completa.
-
Verificações de Utilidades: Confirmando que o local de instalação fornece as utilidades exigidas (energia elétrica, ar comprimido, ventilação de exaustão) e que o ambiente (temperatura, umidade) atende às especificações do fabricante.
-
Instalação de Software: Verificando se o software de marcação e os sistemas de controle foram instalados corretamente e se todos os controles de segurança e de acesso estão devidamente configurados.
Objetivo da IQ: Estabelecer que o equipamento foi instalado corretamente no ambiente previsto e está pronto para operação.
2. Qualificação Operacional (OQ): Definição da Janela Operacional
A fase OQ estabelece que o equipamento de marcação a laser opera de forma consistente dentro das faixas operacionais especificadas. Esta etapa é crucial para definir a "janela segura de operação" para o processo de marcação.
Principais Atividades da OQ:
-
Teste de Parâmetros: Teste sistemático de toda a faixa de parâmetros operacionais críticos, tais como potência do laser, velocidade de marcação, frequência e distância focal.
-
Teste em Cenários de Pior Caso: Teste do equipamento nos limites extremos da faixa operacional (por exemplo, potência mínima e máxima, velocidade mais rápida e mais lenta) para garantir que o sistema continue funcionando corretamente.
-
Teste de Alarmes e Intertravamentos: Verificação do funcionamento conforme projetado de todos os recursos de segurança, alarmes e intertravamentos (por exemplo, intertravamentos de portas, botões de parada de emergência, alarmes de falha na extração de fumos).
-
Teste de Qualidade da Marcação: Geração de marcas de teste em toda a faixa operacional e medição de atributos-chave de qualidade (por exemplo, contraste, profundidade, legibilidade do código) para definir os limites aceitáveis.
Objetivo da OQ: Estabelecer os limites operacionais e demonstrar que o equipamento produzirá resultados aceitáveis quando operado dentro desses limites.
3. Qualificação de Desempenho (PQ): Demonstrar Resultados Consistentes
A fase de PQ é a etapa final e mais crítica, demonstrando que o processo de marcação a laser produz consistentemente resultados aceitáveis sob condições reais ou simuladas de produção, por um período prolongado. Isso aborda diretamente os Requisitos da FDA sobre Identificação Única de Dispositivos (UDI) relativos à permanência e qualidade da marca.
Principais Atividades da PQ:
-
Produção em série: Realização de múltiplas corridas de produção utilizando materiais reais e os parâmetros operacionais definidos (estabelecidos na OQ).
-
Ensaios de Permanência da Marca: Submeter os dispositivos marcados a condições simuladas de uso final, incluindo:
-
Ciclos de esterilização: Autoclave, óxido de etileno (EtO) ou irradiação gama.
-
Limpeza/desinfecção: Exposição repetida a agentes de limpeza e esfregação.
-
Abrão/desgaste: Teste da resistência da marcação a danos físicos.
-
Verificação de rastreabilidade: Garantir que os dados UDI marcados no dispositivo estejam corretamente vinculados aos registros do lote de produção e à base de dados GUDID.
-
Critérios de aceitação: As marcações devem atender consistentemente aos critérios de aceitação predefinidos (por exemplo, níveis de AQL para legibilidade, contraste mínimo e ausência de danos ao material).
Objetivo da validação de desempenho (PQ): Demonstrar, com alto grau de confiança, que o processo de marcação a laser é eficaz e reproduzível nas condições normais de operação, atendendo a todos os padrões de qualidade e regulatórios.
Conclusão: Uma Parceria para a Conformidade
A validação de um sistema de marcação a laser é um processo complexo, em múltiplas etapas, que exige profundo conhecimento técnico e estrita adesão a ISO 13485 e Requisitos da FDA sobre Identificação Única de Dispositivos (UDI) . Escolher um fornecedor de equipamentos a laser capaz de oferecer suporte abrangente à validação — incluindo protocolos detalhados, assistência na execução e relatórios finais — é essencial para garantir rastreabilidade de dispositivos médicos e alcançar a conformidade regulatória. Esse rigoroso processo de validação IQ/OQ/PQ transforma o marcador a laser de um simples equipamento em um processo de fabricação totalmente validado e crítico.
Figura 4: O Processo de Validação em Três Etapas IQ/OQ/PQ