Posted on November 26, 2025
Für Hersteller medizinischer Geräte ist die Einhaltung der Vorschrift zur eindeutigen Gerätekennzeichnung (Unique Device Identification, UDI) der US-amerikanischen Food and Drug Administration (FDA) zwingend vorgeschrieben. Das UDI-System verlangt eine dauerhafte, lesbar angebrachte Kennzeichnung am Gerät oder dessen Verpackung, um die rückverfolgbarkeit medizinischer Geräte und die Patientensicherheit zu verbessern. Da die Lasermarkierung ein Fertigungsprozess ist, der unmittelbar die Qualität des Endprodukts sowie die Einhaltung regulatorischer Anforderungen beeinflusst, müssen sowohl die verwendete Ausrüstung als auch der Prozess selbst gemäß den Vorschriften für Qualitätsmanagementsysteme (Quality System Regulations, QSR) und ISO 13485 normen streng validiert werden. Dieser Artikel beschreibt den wesentlichen dreistufigen Validierungsprozess: Installation Qualification (IQ), Operational Qualification (OQ) und Performance Qualification (PQ).
Die IQ-Phase überprüft, ob die Lasermarkierungsanlage ordnungsgemäß installiert wurde und ob alle erforderlichen Komponenten, Versorgungseinrichtungen und Dokumentation vorhanden sind.
Ziel der IQ: Sicherstellen, dass die Ausrüstung korrekt in der vorgesehenen Umgebung installiert ist und betriebsbereit ist.
Die OQ-Phase stellt sicher, dass die Lasermarkierungsanlage innerhalb der festgelegten Betriebsbereiche konsistent funktioniert. Dieser Schritt ist entscheidend für die Definition des „sicheren Betriebsfensters“ für den Markierungsprozess.
Ziel der Betriebsqualifizierung (OQ): Festlegung der Betriebsgrenzen und Nachweis, dass die Ausrüstung akzeptable Ergebnisse liefert, wenn sie innerhalb dieser Grenzen betrieben wird.
Die PQ-Phase ist der letzte und entscheidendste Schritt, bei dem nachgewiesen wird, dass der Lasermarkierungsprozess unter tatsächlichen oder simulierten Produktionsbedingungen über einen längeren Zeitraum hinweg stets akzeptable Ergebnisse erzielt. Damit wird unmittelbar den FDA-UDI-Anforderungen hinsichtlich Markierungsbeständigkeit und -qualität entsprochen.
Ziel der PQ: Nachzuweisen, dass der Lasermarkierungsprozess unter normalen Betriebsbedingungen mit hoher Zuverlässigkeit wirksam und reproduzierbar ist und sämtliche Qualitäts- und regulatorischen Anforderungen erfüllt.
Die Validierung eines lasermarkiersystem ist ein komplexer, mehrstufiger Prozess, der tiefes technisches Know-how und strikte Einhaltung von ISO 13485 und FDA-UDI-Anforderungen erfordert. Die Auswahl eines Laserausrüstungslieferanten, der umfassende Validierungsunterstützung bietet – einschließlich detaillierter Protokolle, Unterstützung bei der Durchführung sowie abschließender Berichte – ist entscheidend, um rückverfolgbarkeit medizinischer Geräte und die regulatorische Konformität sicherzustellen. Dieser strenge IQ/OQ/PQ-Prozess wandelt das Lasermarkiergerät von einer einfachen Maschine in einen vollständig validierten, kritischen Fertigungsprozess um.
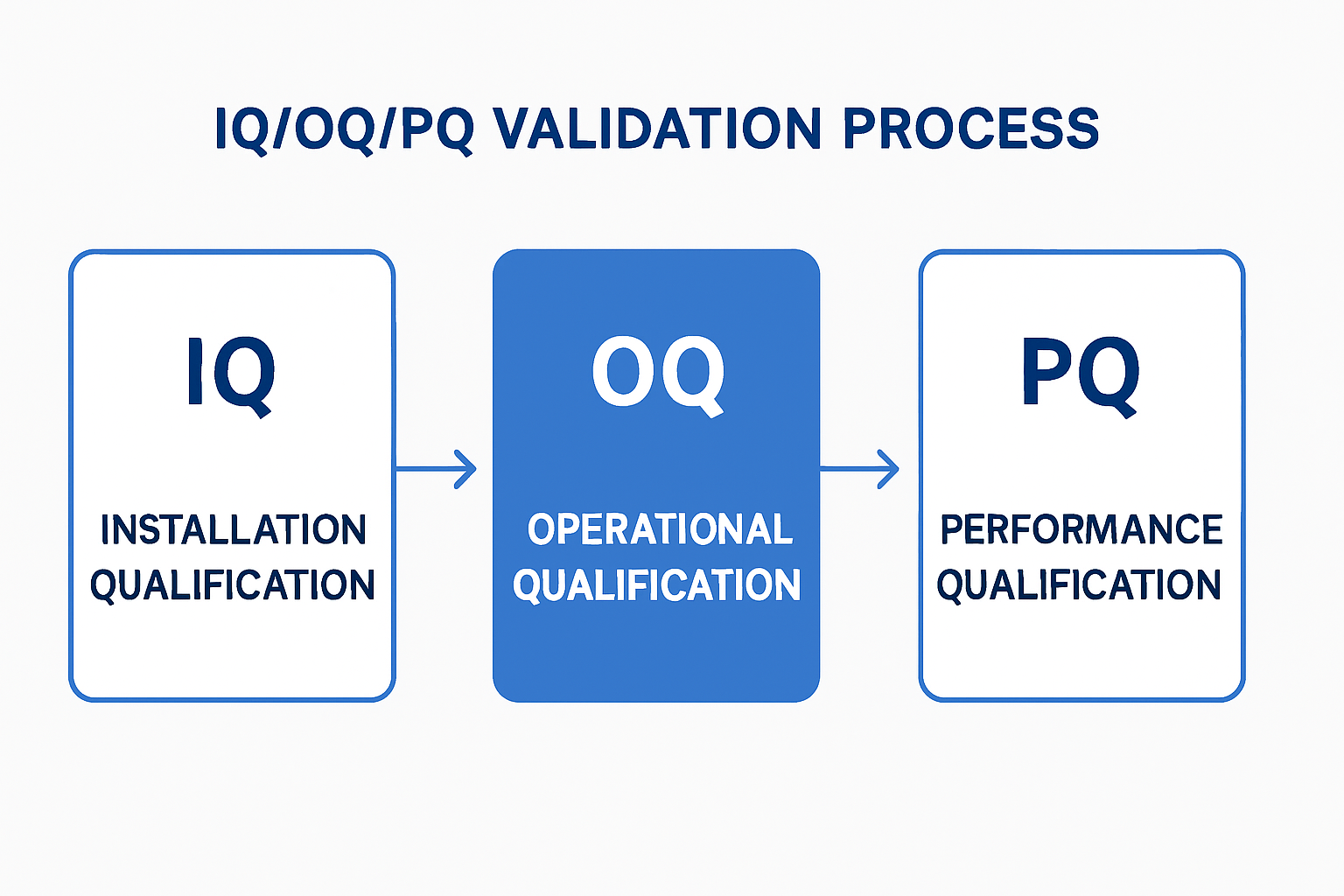
Abbildung 4: Der dreistufige IQ/OQ/PQ-Validierungsprozess